Содержание статьи
Объектом пристального внимания врачей дерматологического и гинекологического профилей считается вирус папилломы человека (ВПЧ). Половые пути и кожа, как наиболее частый ареал обитания данного патогена в организме человека, подвержены высокому риску канцерогенеза, в зависимости от персистирующего типа ДНК ВПЧ.
С тех пор, как в конце прошлого столетия несколькими учёными была обнаружена связь между инфицированием ВПЧ и цервикальным раком, этот вирус стал предметом споров и поводом для волнения среди многих женщин и мужчин.
Генотипы ВПЧ
Рост инфицированности населения эти вирусом определяется двумя причинами:
- Изменение характера сексуального поведения молодых людей: раннее дебютирование половых контактов, значительное количество половых партнёров.
- Совершенствование диагностических методов (гипердиагностика).
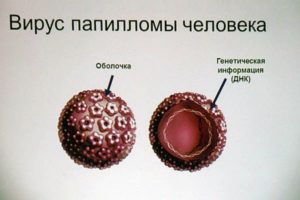
Геном ВПЧ представлен молекулой ДНК. В зависимости от последовательности нуклеотидов в этой молекуле, выделяют множество генотипов. Благодаря современным молекулярно-биологическим методам удалось идентифицировать более 100 генотипов вируса. Около 80 типов описаны подробно и известно, что каждый генотип поражает определённый вид эпителия.
Вирус имеет сродство к различным видам эпителиальной ткани (кожа, слизистые оболочки).
Не все вирусные частицы способны вызвать онкологический процесс. ВПЧ принято делить на высокоонкогенные и низкоонкогенные виды:
- К вирусам, способным вызвать рак, относят следующие типы: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 67, 68.
- К вирусам с низким канцерогенным риском относят: 5, 6, 7, 8, 11, 12, 14, 15, 17, 19, 20, 21, 22, 23, 24, 25, 42, 43, 44.
Наиболее часто высокоонкогенные штаммы обнаруживают при таких заболеваниях шеечного отдела матки, как эктопия, эрозия, лейкоплакия, а в 95-100% случаев их идентифицируют при раке шейки матки.
 Проявления папилломавирусной инфекции:
Проявления папилломавирусной инфекции:
- Бородавки (папилломы) на коже обеспечивают генотипы 1-4, 7, 10, 26-29, 41, 48, 49, 57, 60.
- Эпидермодисплазии (предрак кожи) способствуют генотипы 5, 8, 9, 12, 14, 15, 17, 19, 20-25, 36, 38, 47, 50.
- Верхняя часть дыхательных путей и слизистая оболочка глаза – генотипы 2, 6, 11, 13, 16, 32.
- Бородавки (кондиломы) аногенитальной области – генотипы 2, 6, 11, 16, 18, 30, 40-42, 44, 45, 54, 55, 61.
В свою очередь, итогом персистенции высокоонкогенного ВПЧ будет являться рак различной локализации:
- Карцинома анальной области.
- Злокачественная опухоль шейки матки, влагалища и вульвы.
- Рак полового члена.
- Рак глотки.
16 тип ВПЧ делят на 3 варианта происхождения по континентам:
- Азиатско-американский.
- Североамериканский.
- Европейский.
Активность генов, кодирующих белки трансформации здоровых клеток в опухолевые, у азиатского и североамериканского вариантов очень высокая. По сравнению с европейским вариантом, риск рака при инфицировании этими вариантами возрастает в 11 раз.
Современные методы обнаружения ВПЧ
 Основными методами качественного и количественного определения, генотипирования на сегодняшний день являются:
Основными методами качественного и количественного определения, генотипирования на сегодняшний день являются:
- Качественная идентификация методом ПЦР, где устанавливается факт инфицирования: определяется наличие ДНК ВПЧ различных типов в биологическом материале.Анализ ПЦР может проводиться по двум направлениям:
- С определением генотипа, когда поиск направлен на конкретный тип и в результате указано, каким именно инфицирован пациент, например, 16 типа, 18 типа и т.д.
- Без определения генотипа, когда устанавливается факт наличия в биологическом материале пациента группы высокоонкогенных вирусных частиц, тогда в результате анализа указывают присутствие таких ВПЧ, без определения конкретного генотипа. Обычно такое исследование носит скрининговый характер.
- Digene тест с технологией hybrid capture, который представляет собой ПЦР в режиме real time с количественным определением ДНК (вирусная нагрузка), исследованием экспрессии онкогенов для выявления физического статуса ДНК.
Количественное определение данного патогена (или вирусная нагрузка) имеет большое значение в прогнозе исхода инфицирования. Незначительное количество вирионов неспособно привести к злокачественной трансформации.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Диагностические стандарты папилломавирусной инфекции
Помимо непосредственной идентификации вируса, его количества, важным является определение изменений в клетках эпителия цервикального канала: исследование на наличие атипичных клеток. Это достигается проведением ПАП-теста.
ПАП-тест (методика Папаниколау) определяет наличие атипичных клеток в цервикальном канале. Результаты теста делят на 5 видов:
- Нормальные клетки.
- Признаки воспаления.
- Единичные клетки с атипией, требующие быстрого исследования на рак.
- Наличие атипичных клеток, подозрительных на злокачественный процесс.
- Большое количество атипичных клеток, плоскоклеточный рак.
Digene тест в сочетании с ПАП-тестом являются «золотым стандартом» в доклинических методах верификации заболеваний шейки матки. При невозможности выполнения Digene теста, его заменяют методом ПЦР (качественным и количественным).
Дополнительно проводится кольпоскопия.
Определение локализации вириона в определённой части клетки (свободное состояние или интеграция) является важным моментом диагностирования заболеваний, ассоциированных с ВПЧ:
- Интегрированная фаза: в раковых клетках ДНК вируса встраивается в ДНК человеческой клетки, т.к. высокоонкогенный вирус способен к интеграции.
- Эписомальная фаза: ДНК низкоонкогенного ВПЧ находится независимо от генома клетки хозяина.
Определение локализации вириона проводится с помощью иммуногистохимического метода.<
Патогенез папилломавирусной инфекции
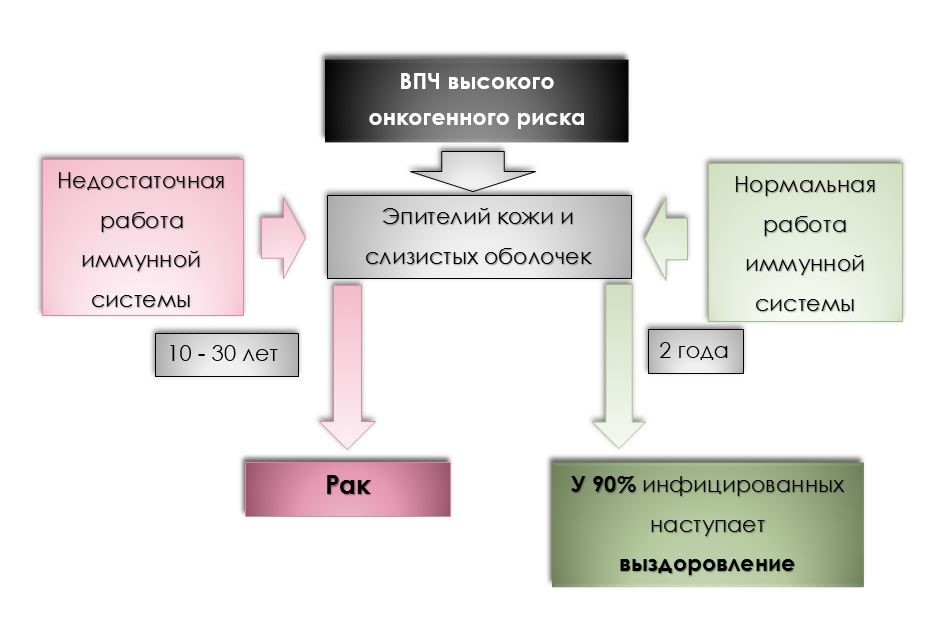
В слизистую оболочку и эпителий молодой кожи вирус попадает беспрепятственно, а для внедрения в кожный эпителий взрослого человека ему необходимы небольшие повреждения.
- При попадании вируса в эпителий клеток кожи и слизистых оболочек, вирусная частица должна достигнуть самого нижнего базального слоя. Этот слой ещё не дифференцирован, он является родоначальником всех клеток эпителия. Вирус нарушает правильную дифференцировку клеток, приводя к росту трансформированных изменённых клеток.
- В роговом слое кожи или поверхностном слое слизистой оболочки происходит сборка новых вирионов – происходит полный репродуктивный цикл ВПЧ: он должен пройти от нижнего к верхнему слою эпителия.
- В верхнем слое вирус ещё не интегрируется в клеточный геном. На этой стадии иммунная система способна побороть патоген и заболевание не возникает – происходит элиминация вируса из организма человека.
- Если иммунитет не справился с вирусом, то, в зависимости от генотипа вируса, развивается его персистенция, что приводит к развитию доброкачественного или злокачественного процесса.
ВПЧ по степени риска онкологического процесса отличаются расположением их в клетке и способности к встраиванию в геном человека.
Высокоонкогенные штаммы на этапе завершения своей репродукции в поверхностных слоях эпителия уже обладают способностью к интеграции, чем и отличаются от низкоонкогенного ВПЧ. Это обеспечивается присутствием в их ДНК особых генов, находящихся в локусах Е6 и Е7. Онкобелки, кодирующиеся этими генами, нивелируют действие человеческих белков, обеспечивающих разрушение (апоптоз) раковых клеток. Таким образом, атипичные клетки не уничтожаются, а продолжают расти и размножаться.
Процесс развития злокачественной опухоли длительный и может занимать не один десяток лет.
Варианты исхода инфицирования высокоонкогенным ВПЧ
В искусственных условиях ВПЧ не культивируется, поэтому механизм канцерогенеза изучен не до конца. Известно, что вирусная ДНК не интегрируется с геномом клетки человека при первой встрече. Именно поэтому против данного вируса эффективна вакцинация. С превентивной целью проводится вакцинация препаратами Гардасил (6, 11, 16, 18 типы) и Церварикс (16 и 18 типы).